- 연골보조 영양제, 과도한 섭취 시 관절염 악화 가능성 확인 -
- 당 생물학과 연골 노화 연관 염증반응의 연관성을 규명한 연구결과 발표 -
[연구필요성]
퇴행성관절염은 가장 흔히 발병하는 질환으로, 막대한 사회경제적 부담을 초래하고 있다. 퇴행성관절염은 세계 인구의 7%에 영향을 미치며, 1990년부터 2019년까지 보면 세계적으로 질환을 앓는 환자 수가 약 48% 증가했다. 노화, 비만, 기계적 과부하, 걸음걸이를 포함하여 위험 요인들이 발병과 가속화에 기여하는 것으로 알려져 있다. 가장 흔한 증상으로 알려진 연골 퇴행과 관절 간격 감소 현상 뿐만 아니라, 퇴행성관절염은 연골하골 경화(subchondral bone sclerosis), 골극 형성(osteophyte formation), 활막염 (synovitis) 등의 병리학적 변화를 동반한다. 연골의 퇴행으로 인해 관절을 움직일 때마다 통증, 움직임의 제한 등이 동반되기 때문에 환자의 삶의 질이 크게 떨어진다. 고령화에 따라 환자 수가 증가하고 있음에도 불구하고 수술이나 통증 완화 치료 이외에 근본적 치료제 (DMOAD, Disease-modifying osteoarthritis drug)가 없다는 점이 연구 개발이 필요한 이유다.
본 연구진은 선도연구센터 (SRC) 사업 당 수식화 네트워크 연구센터 (GNRC)의 구성원으로, 당 연구센터는 O-GlcNAc 수식화를 조절하여 그 기능을 제어하는 기술을 개발하고, 질병 특이적 치료기술 개발에 필요한 기초 연구 자료를 제공하는 역할을 수행해왔다.
[연구성과/기대효과]
1. 연구성과
본 연구성과의 생명과학적 의의는 다음과 같다. 본 연구진은 연골의 기질을 구성하면서 O-GlcNAc 당 수식화의 재료로 사용되는 당 뉴클레오타이드 (nucleotide sugar) UDP-GlcNAc 분자의 분포 및 이동에 관여하는 특정 수송체들의 발현이 퇴행성관절염 연골에서 현저히 감소한다는 사실을 확인했다. 이로 인해 UDP-GlcNAc이 분비성 세포소기관인 소포체나 골지체 대신 세포질에 축적되고 단백질 O-GlcNAcylation이 증가하여 GATA4 단백질이 안정화되는 현상을 발견했다. 이러한 GATA4의 축적은 노화 연관 염증반응을 유도하여 관절염을 악화시켰다. GATA4를 제거하거나 O-GlcNAc 수식화 효소를 억제하여 GATA4 O-GlcNAcylation을 제어하면 퇴행성관절염의 진행을 완화할 수 있음을 동물실험을 통해 확인했다.
본 연구성과의 중개의학적 의의는 다음과 같다. 또한 이번 연구는 연골의 노화에 따른 세포대사 변화와 단백질 조절이라는 분자생물학적 관점에서 퇴행성관절염의 병리 기전을 밝혀 중개의학적 관점에서 중요한 발견으로 평가된다. UDP-GlcNAc의 세포 내 분포와 O-GlcNAcylation이 노화 연관 염증반응을 유도하고 관절염을 악화한다는 사실은 질병의 근본적 원인을 겨냥한 표적 치료제 개발의 가능성을 제시한다. 관절염 진행을 억제하거나 되돌리는 혁신적 치료 접근법으로 이어질 기초를 마련했으며, 약물 개발을 위한 새로운 바이오마커 및 치료표적 발굴에 기여했다는 의의가 있다.
2. 기대효과
본 연구는 퇴행성관절염의 주요 원인으로 알려진 세포노화 현상과 염증반응을 억제하여 퇴행성관절염의 새로운 치료전략을 개발할 가능성을 제시하였다. 특히 UDP-GlcNAc 대사 경로와 O-GlcNAc 당 수식화 조절을 통해 염증반응을 억제하고 퇴행성관절염의 진행을 늦출 수 있다는 점에서 치료표적 발굴 및 치료약물 개발의 새로운 접근법을 제시하였다. 본 연구진의 이번 발견은 현재 사용되는 대증요법 중심의 치료를 넘어 퇴행성관절염의 근본적 원인을 겨냥하는 새로운 세노스태틱 (senostatic) 치료제 개발의 발판을 제공한다. 더 나아가 이미 도래한 초고령화 사회에서 퇴행성관절염 환자들의 삶의 질 향상에 기여할 것으로 기대된다.
서울대 생명과학부 김진홍 교수는 “서울대학교와 연세대학교로 이루어진 노화 및 당 수식화 연구팀과 임상 연구진의 긴밀한 공동연구가 있었기에 가능했던 연구”라며, “우리가 매일같이 섭취하는 당과 건강보조제가 퇴행성관절염의 관리에 영향을 줄 수 있다는 연구결과라는 점에서 큰 의의가 있다”고 밝혔다.
[본문]
□ 개요
최근 국내 연구진이 당 수식화에 의한 연골 노화와 퇴행성관절염 가속화 현상을 새롭게 밝혀내 퇴행성관절염의 병인 기전을 이해하고 질병 치료의 표적을 발굴하는 데 중요한 발견을 했다. 서울대 생명과학부 김진홍 교수와 강동현 연구교수 등이 주도한 연구팀이 “Regulation of senescence-associated secretory phenotypes in osteoarthritis by cytosolic UDP-GlcNAc retention and O-GlcNAcylation”이라는 제목의 논문을 통해 발표한 이번 연구결과는 2025년 2월 4일자로 네이처 커뮤니케이션지에 게재되었다.
지난해 12월 24일 행정안전부의 발표에 따르면 65세 이상 주민등록 인구는 전체 주민등록 인구의 20.0%를 차지하여 한국은 공식적으로 초고령화 사회에 진입하였다. 나이가 들면서 유병률이 증가하는 퇴행성관절염은 관절을 많이 사용하면서 관절 연골이 닳아 없어지는 질병으로, 대한슬관절학회에 따르면 65세 이상 인구의 퇴행성관절염 유병률은 37.8%에 달하며, The Lancet Rheumatology에 발표된 논문에 따르면 2020년 세계 퇴행성관절염 환자 인구는 6억 명에 달한다. 인구의 고령화에 따라 환자의 수가 계속 증가하고 있는 퇴행성관절염은 연골의 퇴행으로 관절을 움직일 때마다 통증, 움직임의 제한 등이 동반되어 환자 삶의 질을 크게 떨어뜨린다.
그러나 질병의 원인을 근본적으로 개선하는 퇴행성관절염의 근본적 치료제 DMOAD (Disease-modifying osteoarthritis drug)는 현재 전무한 상황이다. 퇴행된 연골을 인공관절로 치환하는 인공관절치환술이 현재로서 최선의 방법이지만 이 역시 근본적인 해결책은 되지 못하고 있다. 따라서 퇴행성관절염의 발병 기전의 연구개발을 통해 새로운 치료전략을 발굴하고 유효물질을 확보하는 것은 중요한 과정이다. 이러한 가운데 최근 국내 연구진이 당 수식화를 표적으로 하여 연골세포의 노화를 막고 퇴행성관절염을 완화하는 연구성과를 거둔 것이다.
이번 연구는 제1저자인 강동현 연구교수, 이지연 박사과정 학생을 포함하여 서울대학교 생명과학부 김진홍 교수 연구진이 당 수식화 네트워크 연구센터 (Glycosylation Network Research Center, GNRC), 생명과학부 강찬희 교수 연구진, 서울특별시보라매병원, 분당서울대병원, 이화여자대학교 의과대학과 함께 수행한 이번 연구는 서경배과학재단, 한국연구재단, 국가신약개발사업, 기초과학연구원 등의 지원으로 수행되었다.
□ 기대효과
본 연구는 퇴행성관절염의 주요 원인으로 알려진 세포노화 현상과 염증반응을 억제하여 퇴행성관절염의 새로운 치료전략을 개발할 가능성을 제시하였다. 특히 UDP-GlcNAc 대사 경로와 O-GlcNAc 당 수식화 조절을 통해 염증반응을 억제하고 퇴행성관절염의 진행을 늦출 수 있다는 점에서 치료표적 발굴 및 치료약물 개발의 새로운 접근법을 제시하였다. 본 연구진의 이번 발견은 현재 사용되는 대증요법 중심의 치료법을 넘어 퇴행성관절염의 근본적 원인을 겨냥하는 새로운 세노스태틱 (senostatic) 치료제 개발의 발판을 제공한다. 더 나아가 이미 도래한 초고령화 사회에서 퇴행성관절염 환자들의 삶의 질 향상에 기여할 것으로 기대된다.
서울대학교 생명과학부 김진홍 교수는 “연골세포의 노화와 연골기질의 퇴행을 촉진하는 당 수식화 기전을 밝혔다는 점에서 큰 의의가 있는 연구”라며 “본 연구결과를 바탕으로 연골의 노화를 억제하고 관절을 효과적으로 보호하는 퇴행성관절염 치료전략을 개발할 것”이라는 향후 계획을 밝혔다.
[연구결과]
Regulation of senescence-associated secretory phenotypes in osteoarthritis by cytosolic UDP-GlcNAc retention and O-GlcNAcylation
Donghyun Kang, Jeeyeon Lee, Geunho Yook, Sehan Jeong, Jungkwon Shin, Mi-Sung Kim, Yi-Jun Kim, Hyeryeon Jung, Jinsung Ahn, Tae Woo Kim, Moon Jong Chang, Chong Bum Chang, Seung-Baik Kang, Won Ho Yang, Yong-ho Lee, Jin Won Cho, Eugene C. Yi, Chanhee Kang, and Jin-Hong Kim
(Nature Communications, in press, https://doi.org/10.1038/s41467-024-55085-1)
당 뉴클레오타이드 UDP-GlcNAc은 연골 프로테오글리칸의 글리코사미노글리칸 (glycosaminoglycan, GAG) 사슬 형성을 위한 구성 요소이자 동시에 O-GlcNAcylation의 재료로 기능한다. 본 연구는 UDP-GlcNAc을 소포체와 골지체 등의 분비성 세포소기관으로 운반하는 수송체가 퇴행성관절염 연골에서 크게 감소하는 것에서 출발했으며, 그 결과 연골세포에서 세포질 내 UDP-GlcNAc 축적과 O-GlcNAcylation 증가를 밝혔다. 연구진은 분자생물학적 분석을 통해, 증가한 O-GlcNAcylation이 406번째 serine 아미노산에 부착되어 GATA4를 안정화하며, 이는 p62가 매개하는 선택적 자가포식 (selective autophagy)을 통한 분해를 저해함으로써 노화 연관 염증반응 (senescence-associated secretory phenotype, SASP)의 증가로 이어짐을 밝혔다. 퇴행성관절염 연골의 표면 부분에서 주로 증가하는 O-GlcNAcylation은 GATA4 발현의 증가로 이어졌으며, 이 연골층에서 GATA4를 국소적으로 억제하는 것만으로도 퇴행성관절염이 완화되었다. 또한, O-GlcNAc 수식화 효소를 억제하는 것으로도 GATA4의 발현이 감소하여 퇴행성관절염이 완화되었다. 반대로 글루코사민 과잉 식이 모델을 통해 연골의 O-GlcNAc 수식화를 증가시키면 연골세포에서 GATA4를 안정화되고 퇴행성관절염을 악화시켰다. 이는 관절 보호 목적으로 글루코사민을 복용할 때 과도하게 복용하지 말아야 한다는 가이드라인을 제시하기도 한다. 본 연구결과는 관절의 만성 염증과 연관된 분비 경로를 조절하는 데 있어 UDP-GlcNAc의 세포 내 분포가 중요한 역할을 한다는 점을 밝히면서, 퇴행성관절염 치료를 위한 노화억제 (senostatic) 전략을 제공한다.
- ○퇴행성관절염 (osteoarthritis): 퇴행성관절염은 관절을 보호하는 연골의 감소나 기질 구성성분의 변화로 인해 관절 연골이 파괴되고 극심한 통증이 발생하는 질환이다. 퇴행성관절염의 병리적 원인으로 노화와 같은 생득적 요인이나 비만 및 외상 등 물리적 요인이 지목되고 있으나 근본적 치료제 DMOAD 개발을 위한 연구개발이 지속되고 있다.
- ○연골 (cartilage): 연골조직은 뼈와 뼈 사이에 위치하는 물렁뼈로, 물 분자를 흡수하여 부풀어 올라 완충 작용을 수행하고 뼈를 보호하는 역할을 한다. 걷거나 관절을 움직일 때 연골조직에 가해지는 충격 (인장력, 압축력 등)에 대해 견디기 위해 제2형 콜라겐, 히알루론산, 프로테오글리칸 등이 복잡하게 얽힌 두꺼운 세포외기질 구조를 가진다.
- ○O-GlcNAc 당 수식화 (O-GlcNAcylation): O-GlcNAc 당 수식화는 세포 안에서 일어나는 특별한 당 분자 장식으로, 세포는 특정 단백질의 기능을 조절하기 위해 특정한 위치에 작은 당 분자를 붙였다 떼었다 한다. 이러한 수식화는 세포가 외부 신호에 반응하거나 자신의 상태를 유지하는 데 필요한 현상이다. 세포가 건강하지 않거나 당을 이용해 생물학적 현상을 조절하는 시스템이 균형을 잃는 경우 당 수식화가 과도하거나 부족해지게 되며, 이는 염증반응 활성화, 세포노화 촉진 등을 유발하여 질병으로 이어질 수 있다.
- ○네이처 커뮤니케이션 (Nature Communications): 네이처 커뮤니케이션誌는 세계적 권위의 학술지인 네이처誌의 자연과학 전문 자매지로 Nature Portfolio에서 발행한다. 가장 대표적인 오픈 액세스 (open access) 종합 과학 저널로 평가된다.
[그림설명]
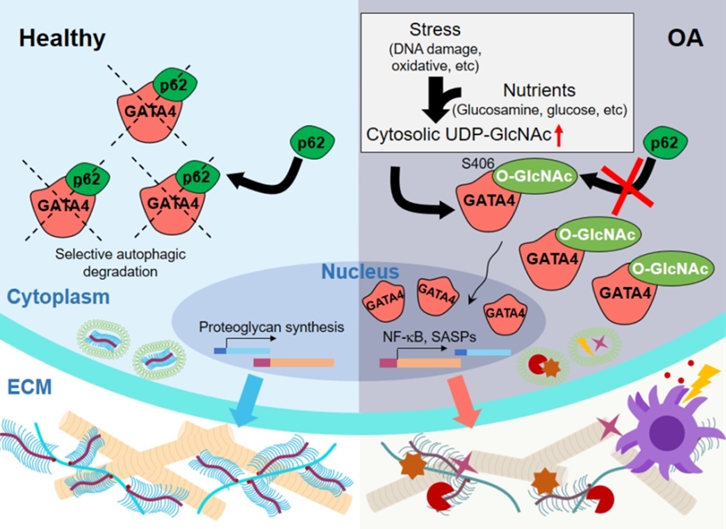
연골세포 내 UDP-GlcNAc 대사와 O-GlcNAc 당 수식화에 의해 노화 연관 염증반응과 퇴행성관절염이 심화되는 기전: 건강한 연골세포에서는 p62 매개 선택적 자가포식에 의해 GATA4가 지속적으로 제거되고, 연골세포는 본연의 기능인 연골기질 합성에 많은 에너지를 사용한다. 반면, DNA 손상, 활성산소, 노화 등 스트레스 상황에서 연골세포 내 UDP-GlcNAc 분포가 세포질에 축적되어 연골기질 합성이 감소하는 반면 오히려 O-GlcNAc 수식화는 증가한다. 그 결과, 제거되어야 할 GATA4가 안정화되어 노화 연관 염증반응이 증가하고 이는 퇴행성관절염을 악화시킨다. 따라서 GATA4를 제거하거나 O-GlcNAc 수식화 효소를 억제하여 GATA4 O-GlcNAcylation을 제어하면 퇴행성관절염의 진행을 완화할 수 있다.

