- 천연물 구조, 생합성 유전자, 항결핵 활성, 작용 메커니즘, 기존 항결핵제와 시너지 효과 등 다학제적 신약개발 연구 -
[연구필요성]
결핵 (Tuberculosis ; TB)은 Mycobacterium tuberculosis (Mtb)에 의해 발생하는 치명적인 감염병으로, 특히 1차 항생제 치료 약물에 대한 내성을 가진 다제내성 결핵은 개발도상국에서 공중보건에 큰 위협이 되고 있다. 따라서 다제내성 및 광범위 약제내성 결핵에 대한 혁신적인 치료법의 필요성 어느 때보다 중요하게 대두되고 있다.
[연구성과/기대효과]
항생제 내성 결핵 치료에 사용할 수 있는 치료제는 매우 제한적이다. 이러한 상황에서 곤충 공생 박테리아 유래 천연물인 아레니콜라이드 A (Ar-A)는 새로운 결핵 치료제 선도물질로서의 가능성을 보여줄 뿐만 아니라, 기존 항결핵제와의 병용 치료를 통해 치료 요법의 단순화 및 치료 기간 단축의 가능성을 제시한다.
[본문]
□ 개요
서울대학교 약학대학 천연물과학연구소 오동찬 교수 연구팀, 경상국립대학교 생명과학부 장지찬 교수 연구팀, 충남대학교 의과대학 조은경, 백승화 교수 연구팀은 딱정벌레목 곤충인 남가뢰 공생 박테리아 유래 천연물로부터 다제내성 결핵균을 살균하는 항생물질을 발굴하였다고 보고하였다. 본 연구결과는 세계 최정상급 화학 학술지인 독일 화학회지 (Angewandte Chemie International Edition, 피인용지수 16.1)에“Arenicolide Family Macrolides Provide a New Therapeutic Lead Combating Multidrug-resistant Tuberculosis”라는 제목으로 게재되었다. (doi/10.1002/anie.202412994 / 공동 제1저자: 서울대학교 약학대학 황성훈 박사, 경상국립대학교 박사과정 허보은, Thanh Quang Nguyen 박사, 충남대학교 박사과정 김영재 / 교신저자: 백승화, 조은경, 장지찬, 오동찬 교수)
□ 연구배경
결핵 (Tuberculosis ; TB)은 Mycobacterium tuberculosis (Mtb)에 의해 발생하는 치명적인 감염병으로, 수천 년 동안 인간을 괴롭혀 왔다. 이 질병은 주로 폐에서 나타나며(약 85%의 사례), 혈류나 림프관을 통해 다른 장기로 퍼질 수 있다. 결핵 치료는 장기적인 치료가 필요하고, 종종 여러 항생제를 조합하여 장기간 복용해야 한다. 치료 중단은 약제내성으로 이어질 수 있으며, 이는 질병의 치료를 더욱 어렵게 만든다. 리팜피신(RFP)과 아이소니아지드(INH) 등의 1차 항생제는 각각 DNA 의존적 RNA 중합효소와 결핵균의 세포벽을 표적으로 하여 결핵균을 사멸한다. 그러나 이러한 1차 항생제 치료 약물에 대한 내성을 가진 다제내성 결핵은 개발도상국에서 공중보건에 큰 위협이 되고 있다.
특히 광범위 약제내성 결핵은 치료에 수년이 걸리며, 이로 인해 상당한 사회경제적 부담과 높은 치명률을 초래하는 매우 심각한 질병이다. 따라서 다제내성 및 광범위 약제내성 결핵에 대한 혁신적인 치료법의 필요성 어느 때보다 중요하게 대두되고 있다.
□ 연구결과
Arenicolide Family Macrolides Provide a New Therapeutic Lead Combating Multidrug-resistant Tuberculosis
Sunghoon Hwang, Bo Eun Heo, Thanh Quang Nguyen, Young Jae Kim, Sung-Gwon Lee, Thanh-Hau Huynh, Eunji Kim, Shin-Il Jo, Min-Jun Baek, Eun-Kyung Shin, Joonseok Oh, Chungoo Park, Yeo Joon Yoon, Eun-Jin Park, Kyung Tae Kim, Sungweon Ryoo, Da-Gyum Lee, Connor Wood, Minjeong Woo, Dae-Duk Kim, Seungwha Paik, Eun-Kyeong Jo, Jichan Jang, Dong-Chan Oh
(Angewandte Chemie International Edition, https://doi.org/10.1002/anie.202412994)
본 연구진은 다제내성 및 광범위 약제내성 결핵균의 생장을 억제하는 새로운 화합물을 탐색하는 과정에서, 딱정벌레의 장내 박테리아인 마이크로모노스포라가 생산하는 거대환 폴리키타이드 천연물 9종 (“아레니콜라이드”로 명명)을 발견하였다. 분광학적 분석, 유도체화 과정, 양자 역학 기반 분자 모델링, 유전자 분석을 통하여 그동안 밝혀지지 못하였던 거대환 물질 아레니콜라이드 A의 입체구조를 처음으로 완전하게 규명하였으며, 그 신규 유도체들의 구조를 밝혀냈다. 또한 아레니콜라이드를 생산하는 생합성 유전자군 (biosynthetic gene cluster)을 최초로 규명하고, 생합성 과정을 생명정보학적으로 제시하였다.
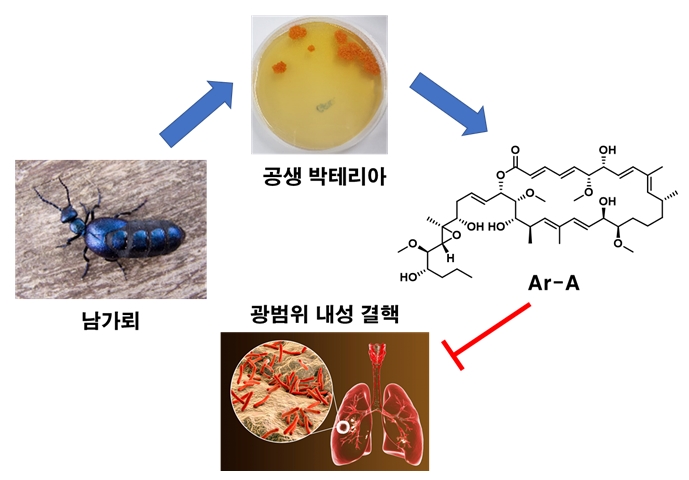
그림 1. 남가뢰 공생 박테리아로부터 광범위 내성 결핵을 제어하는 항결핵제 선도물질 Ar-A를 발굴함.
아레니콜라이드 9종의 물질에 대한 생물학적 평가를 통하여 아레니콜라이드 물질 간 구조-활성 상관관계와 함께 새로운 항결핵 치료제 탐색에서 중요한 돌파구를 제공하였다. 특히 아레니콜라이드 A (Ar-A)는 활발히 증식하는 결핵균뿐만 아니라 치료가 어려운 다제내성 및 광범위 약제내성 결핵균을 포함한 비증식성 변이 결핵균에도 뛰어난 활성을 보였다. 또한 Ar-A는 대식세포 내 및 제브라피시와 설치류 모델에서 결핵균 성장을 억제하고 병변을 완화시키는 효능을 보였다. 본 연구진은 Ar-A가 ATP 고갈을 유도하고 결핵균 세포벽을 불안정하게 하는 이중 작용기전을 가지고 있음을 증명함으로써 기존의 단일 기전 치료제들보다 뛰어난 가치가 있음을 시사하였다. 또한, Ar-A가 MDR-TB의 치료에 사용되는 대표적인 2차 항결핵제인 아미카신(AMK)과의 병용 투여시 치료 상승(synergy) 효과를 일으킬 수 있음을 확인하였다. 이는 Ar-A 병용 투여가 AMK 단독 치료시 야기될 수 있는 긴 치료기간과 신경독성 부작용을 효과적으로 줄일 수 있다는 가능성을 제시한다는 점에서 그 가치가 매우 큰 결과이다. 이에 더하여 Ar-A의 약물동태학적 특성은 이 물질이 경구 투여가 가능하다는 사실을 보여준다. 종합적으로, 본 연구 결과는 Ar-A가 약제내성 결핵 치료를 위한 유망한 항결핵제 선도물질임을 제시하였다.
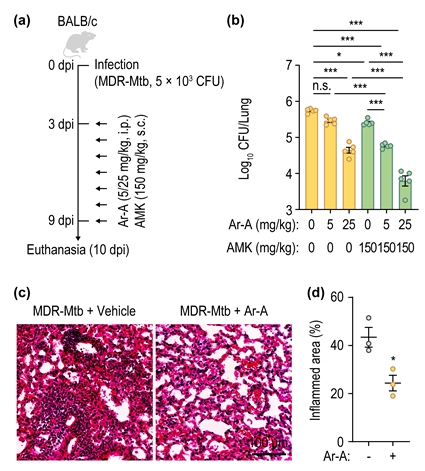
그림 2. 아레티콜라이드 A (Ar-A)와 아미카신 (AMK)의 시너지 효과. (a) 다제내성 결핵 (MDR-Mtb) 감염 마우스 모델에서의 항결핵제 치료요법의 개요 (b) 다제내성 결핵 감염 마우스에서 Ar-A와 AMK 병용 치료시 나타나는 결핵균 감소 효능. (c) Ar-A 투여시 나타내는 다제내성 결핵 감염 마우스에서의 폐병변 감소 효과. (d) 그림 c에서 나타내는 폐염증 소견의 정량적 감소 효과.
결핵은 여전히 전 세계 사망 원인 상위 10위 안에 들며, 단일 감염원으로 인한 사망 원인 중 COVID를 제외하고 HIV/AIDS를 넘어 가장 높은 사망률을 기록하고 있다. 이러한 심각한 공중보건 상황에도 불구하고, 항생제 내성 결핵 치료에 사용할 수 있는 치료제는 매우 제한적이다. 이러한 상황에서 곤충 공생 박테리아 유래 천연물인 아레니콜라이드 A (Ar-A)는 새로운 결핵 치료제 선도물질로서의 가능성을 보여줄 뿐만 아니라, 기존 항결핵제와의 병용 치료를 통해 치료 요법의 단순화 및 치료 기간 단축의 가능성을 제시한다. 이는 세계적으로 가장 치명적인 감염병 중 하나인 결핵의 효과적인 제어와 전파 차단에 기여함으로써 신약개발과 공공 보건에 이바지할 수 있을 것으로 기대된다.
□ 기타
본 연구는 보건복지부의 감염병 예방·치료 기술 개발사업, 과학기술정보통신부의 미생물 제어 및 응용 원천기술개발 사업의 지원을 받아 수행되었다. 또한 한국연구재단의 경상국립대학교 램프(LAMP) 사업 지원을 받아 수행되었다.

