- 팔미트산, 간암 악순환 고리의 방아쇠 -
[연구필요성]
간암은 폐암에 이어 국내 암 사망 원인 2위이며, 현재 간암으로 인한 연간 경제적 부담은 암 중 1위를 차지하고 있음. 따라서 간암 환자 치료에 직접적인 도움을 줄 수 있는 조직학적 바이오마커 발굴이 절실함.
간암 환자의 간에서는 포화지방산이 증가하여 암이 악성화됨. 그러나 과량의 지방산에 의한 암 증식 기전이 제대로 밝혀지지 않아, 근본적 치료가 어려운 상황임.
[연구성과/기대효과]
본 연구는 지방산 중 팔미트산이 간암 세포 내 지방 대사를 변화시켜 간암을 악성화시킴을 밝힘. 그 분자 기전은 팔미트산이 암 억제 단백질인 PHF2를 팔미토일화시켜 단백질 파괴를 유도함을 밝힘. PHF2는 지방 합성을 조절하는 핵심 전사인자인 SREBP1c의 유비퀴틴화 효소로 작용하여 간암 증식을 억제함을 최초로 규명하였음.
연구결과는 팔미트산이 간암 악성화를 초래하는 고리의 원인이 될 수 있음을 밝혀, 향후 간암 환자의 지방식이 제한이 간암 치료의 효과적인 돌파구가 될 수 있음을 시사함.
해당 연구 성과는 세포생물학 분야 저명 국제학술지인 Nature Communications (2022 영향력 지수: 16.6)에 2023년 10월 12일에 게재됨.
[연구결과]
Palmitoylation-driven PHF2 ubiquitination remodels lipid metabolism through the SREBP1c axis in hepatocellular carcinoma
Do-Won Jeong, Jong-Wan Park, Kyeong Seog Kim, Jiyoung Kim, June Huh, Jieun Seo, Ye Lee Kim, Joo-Youn Cho, Kwang-Woong Lee, Junji Fukuda & Yang-Sook Chun
(Nature Communications, https://www.nature.com/articles/s41467-023-42170-0)
연구진은 팔미트산이 간암 세포에서 PHF2를 파괴하여 지방 합성을 촉진하며, 그 분자 기전으로 PHF2가 팔미트산에 의해 팔미토일화된 후 유비퀴틴화에 의해 파괴됨을 밝힘.
PHF2가 간암 세포에서 지방 합성을 지휘하는 주요 전사인자인 SREBP1c의 유비퀴틴화 효소임을 밝혔음. 또한 PHF2를 매개한 SREBP1c의 파괴는 지방산 합성과 암 증식을 모두 억제하였으며, 이는 PHF2의 새로운 기능을 제시한 최초의 연구 결과임.
팔미트산 혹은 PHF2 발현 저하로 인해 SREBP1c 단백질이 증가하면, 이는 팔미트산을 포함한 지방산을 재생산시킴. 팔미트산의 양적 증가는 최종적으로 [팔미트산 ⇒ PHF2 파괴 ⇒ SREBP1c 증가 ⇒ 팔미트산 증가] 악순환 회로를 유도하여 간암을 악성화시킴. 이러한 연구 결과는 간암 환자에게 지방 섭취 제한이 중요함을 시사함.
- ○대사: 생물체가 생명 유지를 위해 진행하는 물질의 분해, 합성과 같은 모든 화학적 변화 과정.
- ○팔미트산: 동식물계에 가장 널리 분포하며, 특히 팜유에 다량으로 함유된 지방산.
- ○팔미토일화: 팔미트산이 표적 단백질에 부착되는 현상.
- ○PHF2: 단백질의 메틸화를 제거하는 탈메틸화 효소로서, 유전자의 발현을 촉진하는 후성유전 조절인자임. 최근 암 억제 기능, 조골세포 분화 촉진, 뇌의 기억/학습 증진 등의 기능을 본 연구진이 밝혔음.
- ○SREBP1c: 간세포에서 지방산 합성을 유도하는 주요 전사인자.
- ○유비퀴틴화: 유비퀴틴 단백질이 표적 단백질에 결합하여 표적 단백질을 파괴하는 현상.
[그림설명]
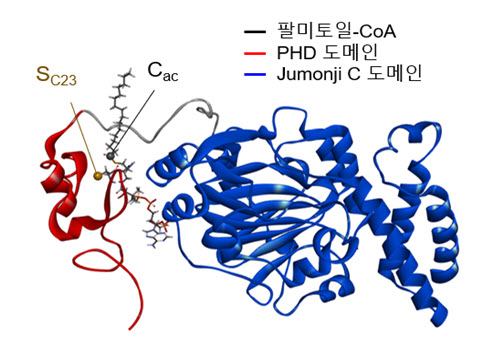
그림1. 팔미토일화 PHF2의 시뮬레이션 구조
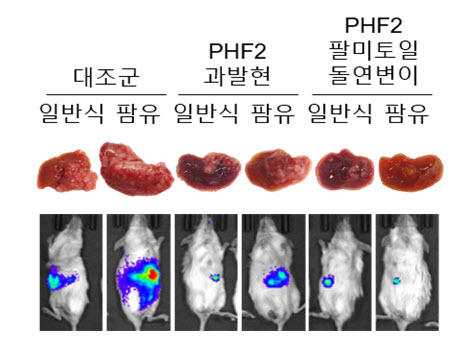
그림2. 팜유 섭취에 의한 암 증식 기전
[그림 2]
그림 2는 형광 표지된 간암 세포의 증식 과정을 촬영한 사진임. 대조군에 비해 팜유 식이 군에서 간암이 급속히 커졌으나, PHF2가 과발현된 세포는 팜유 섭취에 의한 암 증식이 억제됨. 또한, 팔미토일화되지 않는 PHF2 돌연변이 과발현 그룹에서는 팜유 섭취에 의한 암 증식이 관찰되지 않음. 이는 팜유에 의한 간암 증식의 원인이 PHF2를 팔미토일화시켜 단백질 파괴를 유도한 결과임을 시사함.
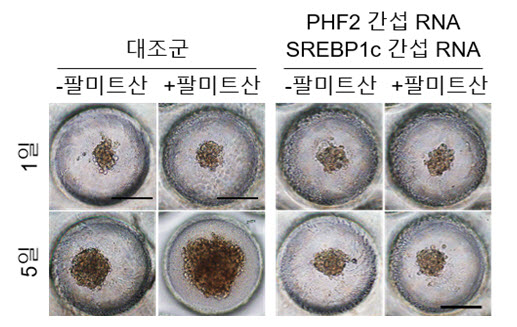
그림3. 팔미트산/PHF2/SREBP1c 이 간암세포 증식을 유도함
[그림 3]
그림 3은 암 미세환경을 구현한 3차원 배양 칩을 통해 암 증식을 추적한 결과임. 간암 세포는 팔미트산에 의해 세포 증식이 유도되지만, SREBP1c 간섭 RNA 조각에 의해 이 간암 세포 증식이 억제됨. 팔미트산-PHF2-SREBP1c 악순환 고리가 간암 악성화의 원인임을 밝힘.
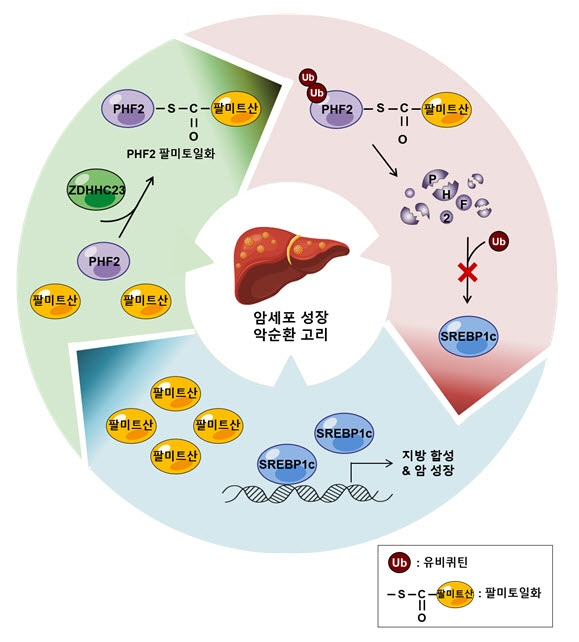
그림 4. 팔미트산⇒PHF2⇒SREBP1c 악순환고리가 간암을 악성화.
[그림 4]
팔미트산이 적은 환경에서는 PHF2가 안정화되어 SREBP1c를 파괴함으로써 지방 합성과 암세포 성장이 저하됨. 그러나, 지방의 과섭취에 의해 팔미트산이 풍부한 환경이 되면 PHF2가 팔미토일화되어 파괴됨으로써, 안정화된 SREBP1c가 팔미트산을 포함한 지방 합성을 다시 증가시킴. 그 결과, 증가된 팔미트산이 간암세포의 증식을 유도하여 간암의 악성화를 초래함.
[핵심내용]
서울대 의대 전양숙 교수 연구팀이 지방산 과섭취에 의한 간암 악성화 기전을 밝혔다.
연구진은 간암의 백서 모델과 암 미세환경을 구현한 3차원 배양 칩을 이용하여, 팔미트산이 간암 세포 증식과 지방 대사를 변환시켜 암을 악성화시킨다는 것을 처음으로 규명하였다.
그 분자 기전으로 팔미트산이 암 억제 단백질인 PHF2를 팔미토일화시켜 단백질 파괴를 유도함을 관찰하였다. 나아가 PHF2가 지방 합성을 조절하는 핵심 전사인자인 SREBP1c의 유비퀴틴화 효소로 작용하여 간암 증식을 억제하고 있음을 밝혔다.
전양숙 교수는 "이번 연구는 지방의 과잉섭취가 간암의 악성화를 초래하는 고리의 방아쇠가 될 수 있음을 밝혔다."라며 "향후 간암 환자의 지방식이 제한이 간암 치료의 효과적인 돌파구가 될 수 있을 것"이라고 이번 성과의 의미를 설명했다.
이번 연구성과는 한국연구재단이 추진하는 중견 연구, 선도연구센터(MRC) 사업의 지원으로 수행되어, 세포생물학 분야 저명 국제학술지인 Nature Communications (영향력 지수: 16.6)에 2023년 10월 12일에 게재되었다.

