- 리소좀 특이적 콜레스테롤의 축적, 노화 연관 염증 반응 촉진 -
[연구필요성]
콜레스테롤은 세포막의 주요 구성 요소로 세포 성장, 분열, 그리고 리모델링에 핵심이 되는 지질체이다. 콜레스테롤 대사의 이상은 암, 치매, 대사증후군, 심혈관 질환, 관절염 등의 다양한 노화 연관 질환 및 노화와 밀접한 연관이 있음이 잘 알려져 있다. 하지만 콜레스테롤 대사 이상이 어떻게 이렇게 광범위한 노화 유발 요소로 작용할 수 있는지는 오랜 기간 동안 수수께끼로 남아있었다. 콜레스테롤 대사 이상에 의한 노화 유발 기전 규명은 이러한 노화 생물학의 난제를 해결할 뿐만 아니라, 차세대 노화 치료제 개발에 실마리를 제공함으로써 21세기 초고령화 사회에 대한 중요한 대책을 마련할 수 있기에 중요하다.
[연구성과/기대효과]
세포 노화는 다양한 스트레스에 의해 유도되는 세포 주기의 정지 반응으로, 여러 염증 인자의 분비를 통해 조직의 기능을 저하하고 노화를 촉진함이 잘 알려져 있다. 본 연구진은 다양한 노화 세포에서 콜레스테롤 대사가 크게 향상되어 있음을 새롭게 확인하였다. 이러한 변화에는 세포 내 콜레스테롤 유출 인자(cholesterol exporter)로 잘 알려진 ABCA1의 발현 증가가 수반되는데, 흥미롭게도 ABCA1 중 일부는 리소좀으로 세포 내 위치를 변경하여 리소좀 콜레스테롤 유입 인자(lysosomal cholesterol importer)로 작용하고 리소좀 내 콜레스테롤 축적을 유도한다. 이러한 리소좀 내 콜레스테롤 축적은 리소좀의 막 구조를 변화시켜, 영양-에너지 대사 경로의 핵심 조절 인자인 mTORC1의 활성을 촉진하고 다양한 염증 유발 분비 인자의 생성을 유도한다. 본 연구진은 ABCA1 표적 약물을 통한 리소좀 내 콜레스테롤 축적의 제어가 노화 연관 염증 반응과 세포 노화를 억제함으로써 대표적인 노화 연관 질환 중 하나인 퇴행성관절염의 증상을 크게 완화할 수 있음을 새롭게 규명하였다.
본 연구는 오랫동안 수수께끼로 남아있던 콜레스테롤의 노화 유발 기전을 세포 노화 및 노화 연관 염증 반응을 통해 밝혔다는데 큰 의의가 있으며, 해당 과정의 제어를 통해 광범위한 노화 연관 질환에 적용할 수 있는 차세대 노화 치료제 개발에 실마리를 제공한다는 점에서 그 중요성이 부각된다.
[본문]
체내의 높은 콜레스테롤 수치는 심장병을 비롯한 다양한 심혈관계 질환을 통해 건강에 악영향을 끼친다. 수많은 역학 조사를 통해 이러한 콜레스테롤의 이상이 노화 및 다양한 노화 연관 질환에서도 관찰됨이 잘 알려졌으나, 그 인과관계는 여전히 수수께끼로 남아있었다. 최근 국내 연구진이 콜레스테롤의 노화 유도 기전을 새롭게 밝혀내, 이러한 난제 해결에 중요한 실마리를 제공하였다. 서울대학교 생명과학부 강찬희∙김진홍 교수가 이끄는 공동 연구진은 3일 세포 노화 및 노화 연관 염증 반응을 일으키는 콜레스테롤의 조절과 작용 원리를 알아냈다고 밝혔다.
세포 노화(cellular senescence)는 정상세포가 스트레스를 받아 분열을 영구히 멈추고, 다양한 염증 인자를 분비하는 현상이다. 최근 노화 세포의 축적이 암, 심혈관계 질환, 퇴행성 질환 등 여러 노화 연관 질환의 주원인으로 작용함이 알려지면서, 노화 세포 표적 기술(senotherapy: 세노테라피)이 차세대 노화 치료제 후보로 세계적인 주목을 받고 있다. 이는 2022년 미국국립보건원(NIH)의 대규모 연구 프로젝트 ‘세포 노화 네트워크(SenNet, $125 million 규모)’ 발족과 제프 베조스(Jeff Bezos) 아마존 창업자의 세포 노화 기반 치료제 개발 회사 알토스랩스(Altos Labs)에 대한 대규모 투자에서 쉽게 알 수 있다. 이처럼 노화 세포의 표적이 ‘인류의 노화에 대한 전쟁’에 있어서 승리의 실마리로 주목받고 있지만, 기술의 상용화를 위해서는 노화 세포의 특성에 대한 심도 있는 이해와 제어법 규명이 필요한 상황이다.
연구진은 이를 위해 노화 세포가 분열하지 않는 세포임에도 불구하고 높은 영양-에너지 대사 경로의 활성을 유지하고 있다는 데 주목하였다. 연구진은 이러한 노화 세포의 특성이 세포 내 ‘분해 공장’으로 알려진 리소좀에 특이하게 축적되는 콜레스테롤에 의해 조절됨을 새롭게 규명하였고, 해당 경로의 억제 시 노화 세포로부터 분비되는 해로운 염증 유발 인자의 생산을 크게 저해할 수 있음을 확인하였다.
연구진은 독자적으로 개발한 ‘초고속 리소좀 분석 기술’을 활용하여 노화 세포의 리소좀 내 콜레스테롤 축적 기전의 핵심 인자 ABCA1 또한 동정하였다. 이렇게 축적된 콜레스테롤은 리소좀의 특이적 구조 변화를 일으켜, 영양-에너지 대사 경로 조절 인자의 상호 결합을 촉진하고 비정상적 활성화를 유도한다. 연구진은 마지막으로 ABCA1의 활성 제어를 통한 노화 연관 염증 인자의 생산 조절이 대표적인 노화 연관 질환인 퇴행성관절염의 증상 완화에 크게 기여할 수 있음을 검증하였다.
강찬희 교수는 “이번 연구 결과는 오랫동안 베일에 싸여있던 콜레스테롤의 노화 유발 기전을 세포 노화 조절을 통해 규명하였다는 데 의의가 있으며, 이를 활용하여 효율적인 노화 세포 표적 전략 수립에 힘쓸 것이다”라며 “리소좀 특이적 콜레스테롤의 축적은 영양-에너지 대사 경로의 이상 조절이 잘 보고된 암세포에서도 일어날 수 있다”라고 밝혔다.
연구의 공동 교신저자인 김진홍 서울대학교 생명과학부 교수는 “리소좀 특이적 ABCA1의 활성 억제제는 노화 연관 염증 반응에 의해 발생하는 퇴행성관절염의 효과적인 치료제로 적용될 수 있다”라며 “해당 억제제는 노화의 기본 단위인 세포 노화를 표적하기에, 더욱 광범위한 노화 연관 질환의 치료제로 개발될 가능성 또한 높다”라고 말했다.
서울대학교 생명과학부 강찬희 교수 연구진이 서울대학교 생명과학부 김진홍∙정종경 교수 연구진 그리고 순천대학교 백만정 교수 연구진과 협업하여 수행한 이번 연구는 서경배과학재단, 한국연구재단, 그리고 삼성미래육성재단의 지원을 받았으며, 대사 분야 최고 국제학술지 ‘네이처 메타볼리즘(Nature Metabolism)’에 3일 공개됐다.
[연구결과]
Lysosomal control of senescence and inflammation through cholesterol partitioning
Kyeonghwan Roh, Jeonghwan Noh, Yeonju Kim, Yeji Jang, Jaejin Kim, Haebeen Choi, Yeonghyeon Lee, Moongi Ji, Donghyun Kang, Mi-Sung Kim, Man-Jeong Paik, Jongkyeong Chung, Jin-Hong Kim, and Chanhee Kang
(Nature Metabolism, in press)
콜레스테롤은 세포막의 주요 구성 요소로 세포 성장, 분열, 그리고 리모델링에 핵심이 되는 지질체이다. 콜레스테롤 대사의 이상은 암, 치매, 대사증후군, 심혈관 질환, 관절염 등의 다양한 노화 연관 질환 및 노화와 밀접한 연관이 있음이 잘 알려져 있다. 하지만 콜레스테롤 대사 이상이 어떻게 이렇게 광범위한 노화 유발 요소로 작용할 수 있는지는 오랜 기간 동안 수수께끼로 남아있었다. 본 연구진은 세포 소기관 중 하나인 리소좀 내 특이적인 콜레스테롤 축적이 노화 세포의 염증 반응을 유지하는 데 중요하며, 이러한 과정을 통해 노화를 촉진할 수 있음을 새롭게 규명하였다.
세포 노화는 다양한 스트레스에 의해 유도되는 세포 주기의 정지 반응으로, 여러 염증 인자의 분비를 통해 조직의 기능을 저하하고 노화를 촉진함이 잘 알려져 있다. 본 연구진은 다양한 노화 세포에서 콜레스테롤 대사가 크게 향상되어 있음을 새롭게 확인하였다. 이러한 변화에는 세포 내 콜레스테롤 유출 인자(cholesterol exporter)로 잘 알려진 ABCA1의 발현 증가가 수반되는데, 흥미롭게도 ABCA1 중 일부는 리소좀으로 세포 내 위치를 변경하여 리소좀 콜레스테롤 유입 인자(lysosomal cholesterol importer)로 작용하고 리소좀 내 콜레스테롤 축적을 유도한다. 이러한 리소좀 내 콜레스테롤 축적은 리소좀의 막 구조를 변화시켜, 영양-에너지 대사 경로의 핵심 조절 인자인 mTORC1의 활성을 촉진하고 다양한 염증 유발 분비 인자의 생성을 유도한다. 본 연구진은 ABCA1 표적 약물을 통한 리소좀 내 콜레스테롤 축적의 제어가 노화 연관 염증 반응과 세포 노화를 억제함으로써 대표적인 노화 연관 질환 중 하나인 퇴행성관절염의 증상을 크게 완화할 수 있음을 새롭게 규명하였다.
본 연구는 오랫동안 수수께끼로 남아있던 콜레스테롤의 노화 유발 기전을 세포 노화 및 노화 연관 염증 반응을 통해 밝혔다는데 큰 의의가 있으며, 해당 과정의 제어를 통해 광범위한 노화 연관 질환에 적용할 수 있는 차세대 노화 치료제 개발에 실마리를 제공한다는 점에서 그 중요성이 부각된다.
[용어설명]
- ○aaaa세포 노화란 다양한 스트레스(예) 텔로미어의 손실, DNA 손상 반응, 활성 산소 스트레스, 종양 유도 스트레스)에 의해 정상 세포가 분열을 비가역적으로 멈추고 다양한 염증 유발 인자를 분비하는 현상을 말한다. 노화 세포의 축적은 주변 정상 세포 및 조직의 기능을 저하하고, 개체의 노화 및 여러 노화 연관 질환을 유발한다. 최근 노화 세포를 제어함으로써 노화를 억제할 수 있다는 것이 보고됨으로써, 세포 노화는 현재 노화 치료제 개발의 표적으로 크게 주목받고 있다.aaa
- ○세포 내 여러 물질(단백질, 지질, 핵산 등)에 대한 분해 효소를 포함하고 있는 세포 내 소기관으로 세포의 분해 공장으로 잘 알려져 있다. 최근 연구에 따르면 리소좀은 이러한 분해 작용뿐만 아니라, 세포 기능 유지 및 성장에 필요한 영양분 및 성장 신호 인자를 인지하고 조절하는 신호 전달 허브로의 기능을 담당한다는 것이 새롭게 보고되고 있다.
- ○노화 세포를 표적하여 노화 및 노화 연관 질환을 늦추고자 하는 차세대 노화 치료 전략을 말한다. 현재 크게는 노화 세포를 특이하게 제거하는 세노라이시스(Senolysis)와 노화 세포로부터 분비되는 해로운 인자의 작용을 억제하는 세노스테틱스/세노몰픽스(Senostatics/Senomorphics) 두 가지 방법이 제시되고 있다.
- ○세포의 기능 유지 및 성장에 필요한 영양분(아미노산, 탄수화물, 지질 등) 및 성장 신호 인자(성장 호르몬)를 인지하고 그 작용을 매개하는 신호 조절 경로로, mTORC1 신호 조절 경로가 대표적으로 알려져 있다.
- ○노화 연관 분비표현형(Senescence-Associated Secretory Phenotype)으로도 불리며, 노화 세포로부터 특이하게 분비되는 다양한 염증 유발 인자를 총칭한다. 주변 세포 및 조직에 노화 신호를 전달하고 기능을 악화시켜, 시스템 수준에서 노화를 촉진하는 것으로 알려져 있다.
[그림설명]
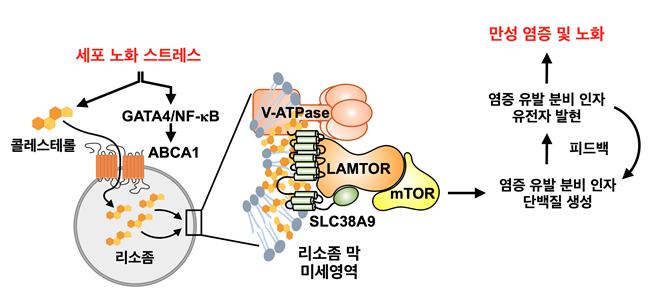
리소좀 특이적 콜레스테롤 축적에 의한 새로운 노화 조절 기전
세포 노화를 유도하는 다양한 스트레스는 노화 세포 내 콜레스테롤 대사를 촉진함과 동시에, 콜레스테롤 유출 인자인 ABCA1의 세포 내 위치를 세포막에서 리소좀으로 변화시킨다. 리소좀에 위치한 ABCA1은 리소좀 콜레스테롤 유입 인자로 작용하며, 리소좀 내 콜레스테롤을 축적하고 리소좀 막 미세영역을 형성한다. 리소좀 막 미세영역은 영양-에너지 대사 경로의 주 조절 인자인 mTORC1의 활성을 강화하고, 염증 유발 분비 인자의 생성 촉진을 통해 만성 염증 및 노화를 일으킨다.

