노화에 따른 셀레늄 대사 감소가 퇴행성관절염의 원인으로 작용한다는 것을 발견,
이에 기반한 치료전략에 대한 실마리 찾아
퇴행성관절염의 원인으로 지목되고 있는 연골세포 노화의 원인이 밝혀졌다. 서울대학교 생명과학부 김진홍‧이병재 교수팀은 “Selenophosphate synthetase 1 deficiency exacerbates osteoarthritis by dysregulating redox homeostasis” 논문을 통해 셀레늄 대사작용에 의한 관절보호 효능을 규명하고 이에 기반한 퇴행성관절염의 치료전략에 대한 실마리를 제시하였다. 본 연구결과는 세계적 학술지인 네이처 커뮤니케이션誌에 2022년 2월 9일자로 게재되었다.
퇴행성관절염은 관절을 많이 사용함에 따라 연골이 닳아 없어지는 질병으로 나이가 들면서 유병률이 증가한다. 연골의 퇴행으로 인해 관절을 움직일 때마다 통증, 움직임의 제한 등이 동반되기 때문에 환자의 삶의 질이 크게 떨어진다. 퇴행성관절염 환자는 세계적으로 60세 이상 인구 29.5%에 달하며, 인구의 고령화에 따라 환자의 수가 계속 증가할 것으로 예상된다.
퇴행성관절염의 근본적 치료제는 전무한 상황이다. 현재로서는 퇴행된 연골을 인공관절로 치환하는 인공관절치환술이 최선의 방법이지만 이 역시 근본적인 해결책은 되지 못하고 있다. 따라서 퇴행성관절염의 발병 기전 연구를 통한 새로운 치료전략의 발굴이 필요하다. 최근 국내 연구팀이 셀레늄 대사의 항산화 개념을 연골조직에 적용하여 연골세포의 노화를 막고 퇴행성관절염을 완화하는 연구성과를 거두었다.
퇴행성관절염은 연골세포 내 산화환원 항상성이 깨지면서 나타나는 세포노화가 원인으로 알려져 있는데, 본 연구팀은 연골세포 내 산화환원 항상성을 유지하는 조절자로서 셀레늄 대사 효소 SEPHS1을 규명하였다. 연구의 제1저자인 강동현 박사와 이지연 박사과정 학생은 퇴행성관절염 연골세포에서 SEPHS1의 발현이 감소하면서 항산화 기능을 가진 셀레늄단백질의 발현이 현저히 줄어들었고, 그 결과 DNA 손상과 세포노화 현상을 동반하면서 퇴행성관절염이 진행되는 것이 관찰되었다. 이러한 병리학적 현상이 항산화제 투여를 통해 사라지는 것을 분자생물학적 수준에서뿐만 아니라 퇴행성관절염 동물모델을 이용한 조직학적, 행동학적 수준에서까지 보임으로써, 연골세포 노화를 막을 수 있는 조절자 SEPHS1을 이용한 퇴행성관절염 치료에의 길을 최초로 제시하였다. 서울대학교 생명과학부 김진홍 교수 연구팀과 이병재 교수 연구팀이 서울특별시보라매병원, 분당서울대병원, 미국 Harvard Medical School, 미국 국립보건원 (NIH) 연구팀과 함께 수행한 이번 연구는 서경배과학재단, 한국연구재단 기초연구사업(중견연구) 등의 지원으로 수행되었다.
본 성과는 항산화 기능이 제시되었던 셀레늄 대사과정과 퇴행성관절염 간의 인과관계를 밝힌 최초의 연구라는 점에서 그 의의가 있다. 또한 SEPHS1의 감소 현상이 노화나 물리적 충격 등의 스트레스를 받은 연골세포의 노화 원인이라는 것을 밝혔다는 데 의미가 있다. 본 연구의 내용은 셀레늄의 식이와 체내 셀레늄 대사 모두가 관절의 건강을 보존하는 데 중요하다는 것을 제시하였다. 셀레늄 식이를 통한 퇴행성관절염 치료전략은 치료제나 수술에 비해 환자에게 진입 장벽이 낮기 때문에 미래에 다양한 계층의 수요를 만족할 수 있을 것으로 기대된다.
서울대학교 생명과학부 이병재 교수는 "세포 내 셀레늄의 대사 이상이 질병의 원인이 된다는 생물학적 근거를 제시했다는 데 큰 의의가 있다”라고 답했다. 서울대학교 생명과학부 김진홍 교수는 “본 연구결과를 바탕으로 관절을 효과적으로 보호할 수 있는 셀레늄 섭취방법을 개발할 것”이라고 향후 계획을 밝혔다.
[연구결과]
Selenophosphate synthetase 1 deficiency exacerbates osteoarthritis by dysregulating redox homeostasis
Donghyun Kang*, Jeeyeon Lee*, Jisu Jung, Bradley A. Carlson, Moon Jong Chang, Chong Bum Chang, Seung-Baik Kang, Byung Cheon Lee, Vadim N. Gladyshev, Dolph L. Hatfield, Byeong Jae Lee†, and Jin-Hong Kim†
(Nature Communications, published in Feb, 2022)
1. 연구 배경
퇴행성관절염 환자는 세계적으로 60세 이상 인구 29.5%, 70세 이상 인구 35.5%에 달하며, 우리나라 65세 이상 인구 퇴행성관절염 유병률은 2017년 기준 30.9%에 달한다. 인구의 고령화에 따라 환자의 수가 계속 증가할 것이 예상되어 퇴행성관절염을 치료하기 위한 표적인자를 발굴해야 한다.
퇴행성관절염은 노화, 외상, 물리적 과부하 등의 위험인자에 의해 발생한다고 알려져 있으며, 가장 두드러지는 증상은 연골의 퇴행과 그로 인해 관절을 움직일 때마다 나타나는 통증, 움직임의 제한 등이다. 연골은 뼈와 뼈 사이에 위치하는 조직으로 물 분자를 흡수하여 부풀어 올라 완충 작용을 수행하고 뼈를 보호한다. 연골은 연골세포에 의해 합성되며, 연골세포에 축적되는 활성산소와 같은 산화 스트레스가 연골세포를 늙게 만들어 퇴행성관절염을 유발하는 주요 원인으로 지목되고 있다. 따라서 연골세포 내 산화 스트레스를 줄인다면 퇴행성관절염을 완화할 수 있다.
셀레늄은 필수 미량원소로 산화환원 항상성을 유지하는 데 꼭 필요하다. 셀레늄은 셀레노시스테인이라는 아미노산 형태로 셀레늄단백질 안에 들어가 체내 산화 스트레스를 제거하는 기능을 한다. 따라서 셀레늄의 대사와 퇴행성관절염의 진행 간에 중요한 연관성이 있을 것으로 예상되고 있다. 셀레늄은 카신벡 병과 같은 풍토병 관절질환에서 치료 효과가 있는 것으로 알려져있지만 셀레늄 대사가 퇴행성관절염에 미치는 영향에 대한 연구는 진행된 바가 없다. 이에 본 연구팀은 셀레늄 대사가 퇴행성관절염에 미치는 영향을 연구하고 항산화제와 셀레늄 식이요법이 퇴행성관절염을 완화하는 효과가 있는지 테스트하였다.
2. 연구 내용
본 연구팀은 퇴행성관절염을 유발하는 활성산소가 증가하는 원인을 밝히는 연구를 진행하였다. SEPHS1은 체내 셀레늄 대사에서 작용하는 효소로, 그 정확한 기능은 아직 알려지지 않았다. 이러한 SEPHS1이 정상 연골세포에서는 잘 발현되지만 퇴행성관절염 연골세포에서는 발현이 현저히 줄어드는 것을 확인하였으며, 셀레늄 대사과정에서 합성되는, 항산화기능을 가지는 셀레늄단백질들의 발현이 SEPHS1의 발현 감소에 따라 확연하게 줄어드는 것을 확인하였다. 이에 따라 연골세포 내 활성산소가 축적되어 DNA 손상과 세포노화 현상이 나타났다. 실제로 퇴행성관절염 질환을 유도한 마우스 모델에서 SEPHS1의 발현을 제거했을 때 질환이 심화되었으며, 셀레늄 결핍 식이를 먹일 시 퇴행성관절염 질환이 더욱 심해지는 것을 분자생물학적, 조직학적, 행동학적 분석을 통해 확인하였다.
이렇게 심해진 퇴행성관절염 질환을 완화시키고자 SEPHS1를 발현하지 않는 마우스 모델에 추가적인 셀레늄을 먹이를 통해 공급했지만 질환의 정도는 개선되지 않았다. 하지만 항산화제로 잘 알려진 N-아세틸시스테인을 먹이자 퇴행성관절염 질환이 완화되는 것을 확인하였다. 이를 통해 셀레늄단백질 합성에 기여하여 활성산소를 제거하는 SEPHS1이 결핍됨으로써 퇴행성관절염 질환이 발병함을 확인하였으며, 그 발병 원인을 밝힘으로써 퇴행성관절염 질환 치료에의 가능성을 열었다는 점에서 의의가 있다.
3. 기대효과 본 연구는 치료제가 퇴행성관절염의 원인으로 알려진 세포노화 현상이 발생하는 근본적인 원인을 밝혀냈다. 특히 현재까지 밝혀지지 않은 연골세포에서의 셀레늄 대사의 중요성을 규명함으로써 퇴행성관절염의 새로운 치료 표적을 확립하였고 보다 효과적이고 용이한 치료법 개발의 실마리를 제공할 것이 기대된다. 이와 같은 연골퇴행의 원인 규명은 연골퇴행을 근본적이고 종합적으로 제어할 식이치료제의 개발과 난치병 치료기술의 상용화로 이어져 국민 복지 향상에 크게 기여할 것이다. 현재 국내 특허등록까지 마무리된 상태로 해당 시장에 혁신적인 발전을 가져올 것으로 기대된다.
[용어설명]
- ○네이처 커뮤니케이션誌는 Nature Publishing Group에서 주관하는 저널로 세계적 권위의 학술지인 네이처誌의 자연과학 전문 자매지이다.
- ○2020년도 IF는 14.919인 정상급 저널이다.
- ○연골조직은 뼈와 뼈 사이에 위치하는 조직으로 물 분자를 흡수하여 부풀어 올라 완충 작용을 수행하고 뼈를 보호한다. 보행하거나 관절을 움직일 때 연골조직에 가해지는 충격(인장력, 압축력)에 대해 견디기 위해 두꺼운 세포외 기질인 제2형 콜라겐과 프로테오글리칸으로 주로 구성되어 있다.
- ○퇴행성관절염은 관절을 보호하는 연골의 감소나 퇴행성 변화로 인해 관절 연골이 파괴되고 극심한 통증이 발생하는 질환이다.
- ○그 병리적 원인으로 노화와 같은 생득적 요인 또는 비만 및 외상 등 물리적 요인에 의해 퇴행성관절염의 발생이 증가하는 것으로 알려져 있다.
- ○우리 몸에 꼭 필요한 미량원소로 적정량을 섭취해야 하며, 부족하면 빈혈, 고혈압, 암 등 질환의 원인이 되기도 한다. 셀레늄은 강력한 항산화 작용을 가지고 있어 몸 속의 자유 라디칼이나 활성산소를 제거한다. 따라서 스트레스에 따른 DNA 손상을 방지하여 세포를 노화로부터 보호하는 기능이 있다. 하지만 적정량을 벗어난 과량을 복용할 경우 독성이 나타날 수 있다. 셀레노시스테인, 셀레노메티오닌 등 아미노산을 구성하며 이러한 아미노산을 포함하는 단백질을 셀레늄단백질으로 구분한다.
[그림설명]
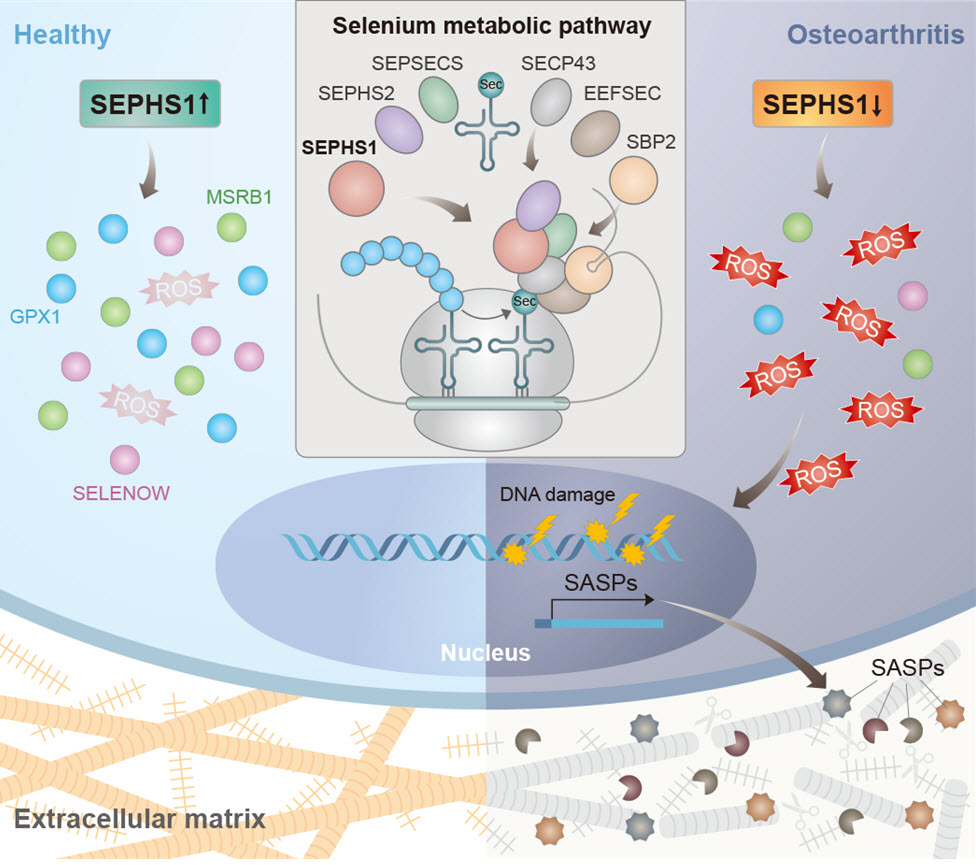
정상 및 퇴행성관절염 연골세포에서의 활성산소 제거 기전
셀레늄 대사에 관여하는 SEPHS1은 항산화 기능을 가진 셀레늄단백질 합성 과정에 참여한다. 그 결과 만들어진 셀레늄단백질들은 활성산소를 제거하여 건강한 연골을 유지할 수 있도록 한다 (왼쪽). 외부 스트레스 상황에서는 SEPHS1이 감소하여 셀레늄단백질의 합성이 저해되고, 활성산소가 증가하여 결과적으로 퇴행성관절염 질환이 유발된다 (오른쪽).

